La reacción de Ritter es una reacción química que transforma un nitrilo en una N-alquilamida usando diversos reactivos alquilantes electrofílicos. Para la reacción original se formó el agente alquilante usando un alqueno en presencia de un ácido fuerte. La reacción ha sido objeto de varias revisiones bibliográficas..[1][2][3][4][5][6][7]
Los alcoholes primarios, secundarios, terciarios, y bencílicos así como el acetato de terbutilo, también reaccionan con éxito con nitrilos en presencia de ácidos fuertes para formar amidas a través de la reacción de Ritter.
Historia
La reacción de Ritter lleva el nombre de John J. Ritter, un químico estadounidense que recibió su doctorado de la Universidad de Columbia. En 1948, P. Paul Minieri, estudiante de Ritter, presentó trabajos sobre la reacción como su tesis doctoral. La reacción todavía tiene importancia hoy en día debido a su aplicabilidad y reproducibilidad para la síntesis de amidas sustituidas con carbonos terciarios.
Mecanismo de reacción
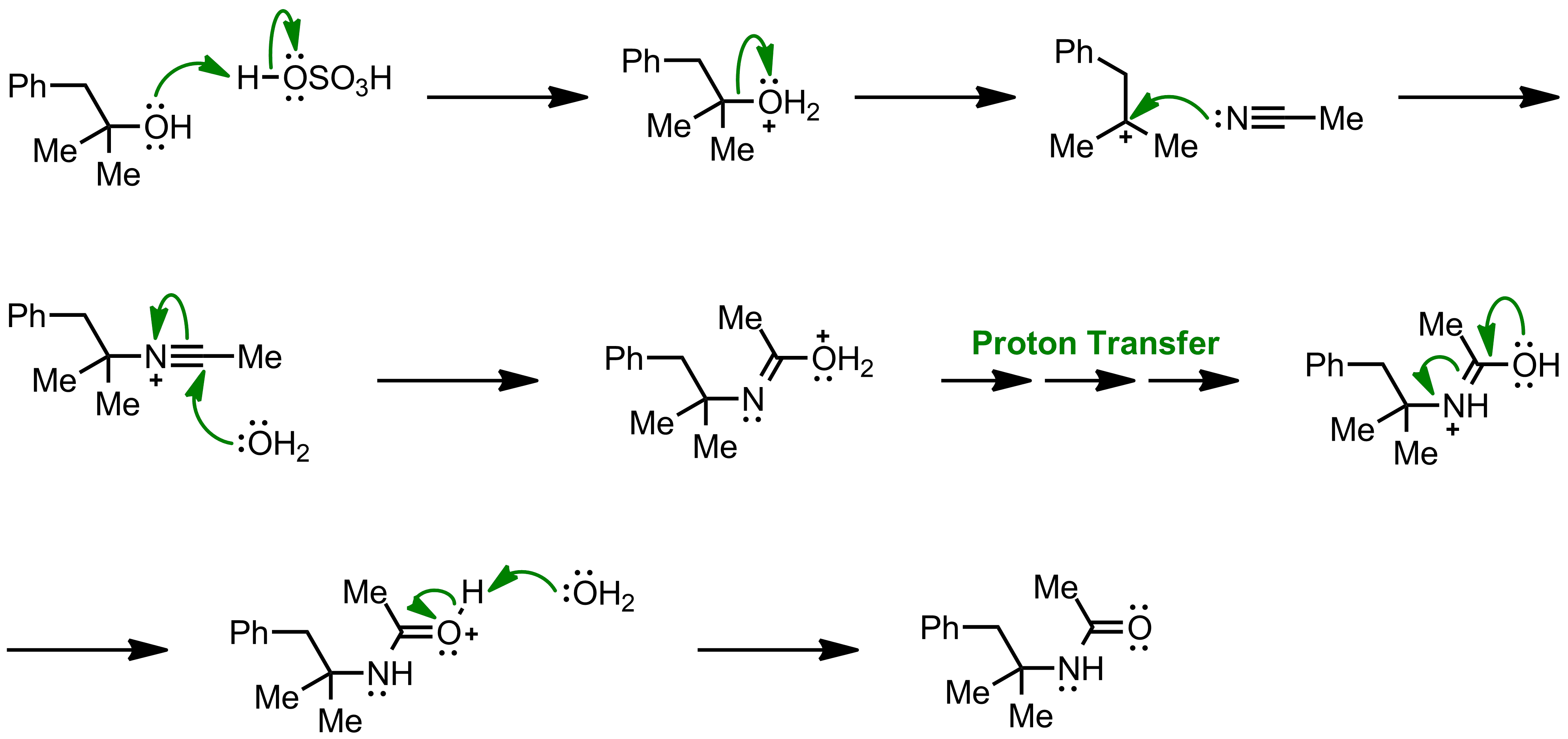
La reacción de Ritter procede por la adición electrofílica del carbocatión 2 para formar el catión nitrilio. El ion nitrilio resultante 3 se hidroliza con agua hasta la amida 5 deseada..[8][9]
Aplicaciones
La reacción de Ritter es más útil en la formación de amidas en las que el nitrógeno tiene un grupo alquilo terciario. También se utiliza en procesos industriales, ya que puede ampliarse eficazmente desde experimentos de laboratorio hasta aplicaciones a gran escala, manteniendo un alto rendimiento. Las aplicaciones del mundo real incluyen la síntesis a escala industrial del fármaco anti-VIH Crixivan (indinavir) de Merck; la producción del inhibidor de falcipain-2 PK 11195; la síntesis del alcaloide aristotelona y la síntesis de amantadina, un fármaco antiviral y antiparkinsoniano. Otras aplicaciones de la reacción de Ritter incluyen la síntesis de ligandos del receptor de la dopamina y la producción de anfetamina del alilbenceno. Un problema con la reacción de Ritter es la necesidad de un catalizador ácido extremadamente fuerte para producir el carbocatión. Este tipo de producto químico corrosivo presenta un riesgo ambiental para los residuos químicos y el riesgo de seguridad para ejecutar la reacción en sí. Sin embargo, se han propuesto otros métodos para promover la formación de carbocationes, incluida la transferencia de electrones fotosensibilizados o la fotólisis dirigida.[10][11][12] [13][14]
Referencias